本年もインフルエンザの季節が近づいてきました。いくら気を付けても周りの環境に依存することも多く、完全な予防というものはなかなか難しいところです。今回は免疫についての話です。
「免疫療法の発見」
2018年ノーベル生理学・医学賞に京都大学の本庶佑(ほんじょ・たすく)特別教授と米テキサス大のJames P.Allison教授が受賞されたことは記憶に新しいと思います。
日本では本庶教授の話題のほうが多いと思いますが、両氏とも免疫という分野こそ共通しているものの、違う機序でガン治療に対する効果を証明しました。
ヒトには自己以外のモノや異物を攻撃する免疫システムが存在しています。これは自己とそれ以外のものを認識する仕組みがあるということであり、自分自身を誤って攻撃してしまうと、自己免疫疾患という形で病気が発症します。
ガン細胞も異物であるためT細胞(免疫細胞)が攻撃しようとしますが、同時に自己からできたモノであるため、T細胞に対して「自己を攻撃しないように」と命令することができます。その為、T細胞はガン細胞への攻撃をやめ、ガンが増殖することになります。
本庶教授の研究は、T細胞への「自己を攻撃しないように」という命令を受け取らないようにする方法を発見(PD-1)したことであり、従来の手術、放射線治療、抗ガン剤に次ぐ4番目の治療方法を提示することができました。
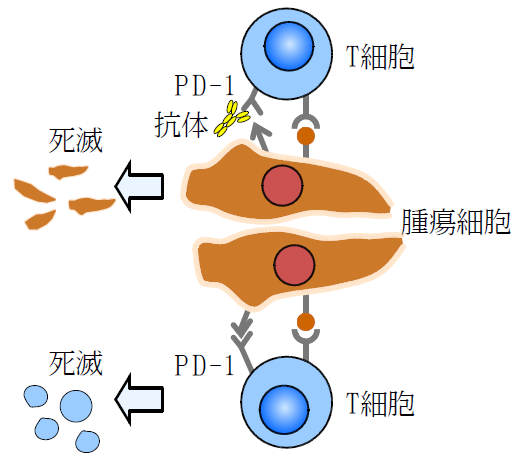 図1 PD-1の作用機序
図1 PD-1の作用機序
本来はT細胞のPD-1受容体にたいして腫瘍細胞が結合しT細胞が自殺するように命令するが、あらかじめPD-1受容体に無害な抗体で蓋をしてしまうことで、腫瘍細胞が結合できなくなる。結果、腫瘍細胞がT細胞の攻撃で死滅する。
一方でAllison教授の研究は、例えば風邪を引いたときにT細胞は増殖しウイルス等を攻撃しますが、あるタイミングで増殖にストップがかかる仕組みを発見(CTLA-4)しました。つまりこのストップに関わる部分を人為的にはずしてしまえば、T細胞は増殖し続けることになります。
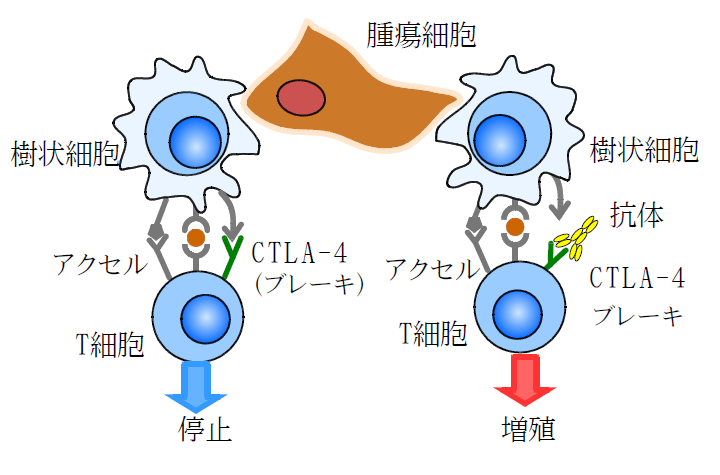
図2 CTLA-4の作用機序
外敵に対する情報を持った樹状細胞が成熟前のT細胞に対して情報を提示、同時に増殖を促す(アクセル)が、ある程度増殖するとCTLA-4(ブレーキ)と結合し、増殖を停止させる。このCTLA-4を無害な抗体で蓋をすることで、さらに増殖を促すことができる。
これら2つの作用機序を利用した薬剤を用いた実験の一例として以下のものがあります。
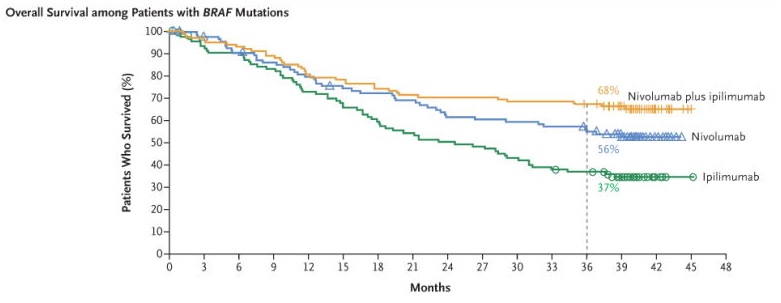
BRAF遺伝子変異を伴うメラノーマ患者の生存率の表1)です。3本のグラフがありますが、下からAllison教授の原理を利用した薬剤、真ん中が本庶教授の原理を利用した薬剤。一番上が両氏の併用です。
縦軸は生存率、横軸は期間を表していますが、それぞれ単独で使用するより併用したほうが生存率は高いことがわかります。T細胞自体を増やし、ガン細胞からの抑制を防ぐのですから、この2つが重なれば効果が大きいことは妥当な結果かと思われます。
いずれにしても、今回注目された免疫療法が、薬剤の力を借りるとはいえ、基本的に本人の免疫力によりガンと対抗できることを示した点が非常に大きなことだと思われます。このように画期的な発見ではあるのですが、薬剤である以上副作用に関しては考慮しなくてはならないようです。
(②に続く)
「参考文献」
1) Wolchok JD, et al. Overall Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma. N Engl J Med. 2017; 377(14): 1345-1356.
